22.07.2020 Wie fixieren Bakterien das Klimagas Kohlendioxid?
Neue Emmy Noether-Nachwuchsgruppe „KryoEM von molekularen Maschinen“ an der Philipps-Universität
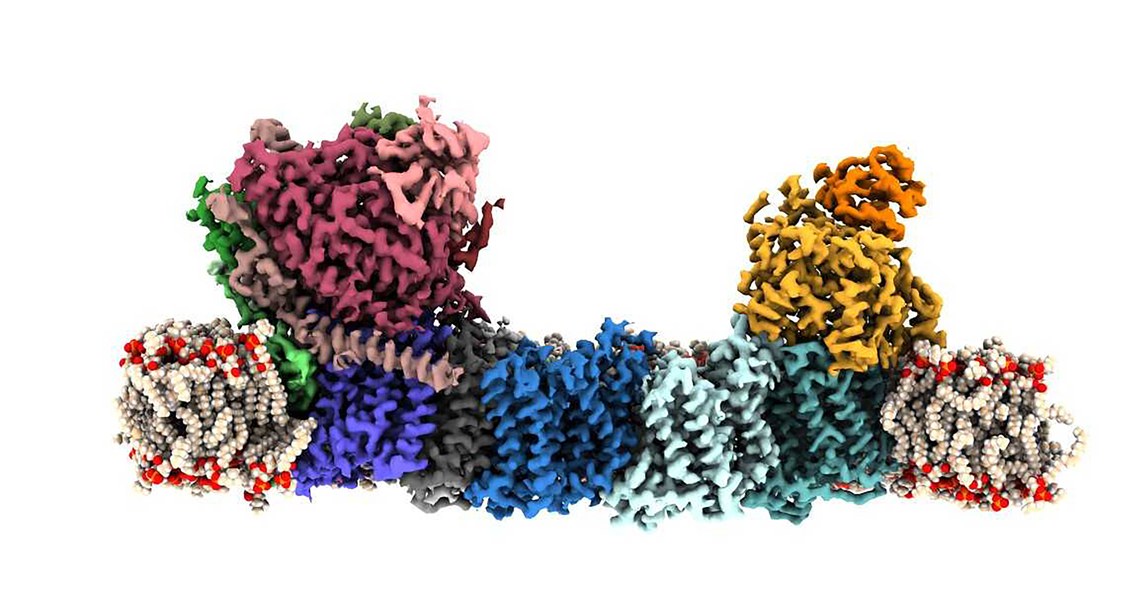
In bakteriellen Zellen führen biologische Makromoleküle eine Vielzahl verschiedenster Aufgaben durch. Manche funktionieren als Speicher von Energie oder Erbinformationen, andere wiederum können Zellen aufbauen und Signale weiterleiten. Eine neue Emmy Noether-Nachwuchsgruppe am Zentrum für synthetische Mikrobiologie (SYNMIKRO) der Philipps-Universität Marburg wird sich in den kommenden sechs Jahren einer besonderen Gruppe von Makromolekülen widmen: Das Forschungsteam unter Leitung von Dr. Jan Michael Schuller vom Fachbereich Chemie der Universität Marburg interessiert sich für biologische Systeme, die für die Kohlenstofffixierung und die Energieumwandlung in bakteriellen Zellen verantwortlich sind. Schuller ist Experte für Kryo-EM, der Kryo-Elektronenmikroskopie. Mithilfe dieser Methode werden die Forscherinnen und Forscher Strukturen von membrangebundenen Multi-Protein-Komplexen hochauflösend bestimmen und für die Synthetische Biologie nutzbar machen. Die Emmy Noether-Nachwuchsgruppe wird von der Deutschen Forschungsgemeinschaft (DFG) mit rund 1,6 Millionen Euro gefördert.

„Diese biochemischen Reaktionen bergen eine Vielzahl von Möglichkeiten für die Synthetische Biologie“, sagt Schuller. „Wir können Sie hoffentlich eines Tages dazu nutzen, um Naturstoffe und solare Brennstoffe aus optimierten photosynthetischen Bakterien herzustellen. Oder aber um gasförmiges CO2 mittels biologischer Organismen aus der Atmosphäre zu binden“, ergänzt Schuller. Seine Gruppe will den Mechanismus von cyanobakteriellen membranständigen Kohlensäureanhydrasen verstehen. „Diese bemerkenswerten Enzyme schaffen es, sehr hohe intrazelluläre Bicarbonat-Konzentrationen zu erzeugen, die als Treibstoff für die Kohlenstofffixierung mittels Rubisco verwendet werden“, sagt Schuller.
Dafür macht sich das Forschungsteam eine Methode zu nutzen, die Schuller in seiner Zeit als Gastwissenschaftler an der Harvard Medical School kennen lernte: In der Kryo-Elektronenmikroskopie (KryoEM) werden Makromoleküle schnell und rasch abgekühlt, sodass sich keine Eiskristalle bilden können. Stattdessen bildet sich verglastes Wasser, in dem die Makromoleküle unbeschädigt eingefroren sind, das aber für Elektronenstrahlen durchsichtig ist. Mit Hilfe eines Elektronenmikroskops können nun Bilder erstellt werden, aus denen mit Hilfe von Computern eine exakte 3D-Struktur des Makromoleküls berechnet werden kann – mit einem Detailreichtum, der mit dem von Röntgenkristall-Strukturen vergleichbar ist. Dieser genaue Blick auf den Aufbau von Biomolekülen ist ein wichtiges Werkzeug, um den katalytischen Mechanismus eines Enzyms zu verstehen und ihn letztlich für biotechnologische Anwendungen nutzbar zu machen.
Vertiefte Kenntnisse über Kryo-EM erlangte Schuller während seiner Promotion am Max-Planck-Institut für Biochemie in Martinsried, wo er sich auf die Einzelpartikelanalyse von Proteinen spezialisierte. „Photosynthetische Bakterien sind faszinierend und können ein wichtiger Faktor in der Bekämpfung der Erderwärmung sein. Das ist definitiv eines der Anwendungsszenarien, die wir in unserem kommenden Projekt stets im Fokus haben werden“, sagt Schuller.
Kontakt
Dr. Jan Michael Schuller
Tel.: 06421 28-22584
Mail: jan.schuller@synmikro.uni-marburg.de
Fachbereich Chemie
Philipps-Universität Marburg