Hauptinhalt
Ausblick
Ein Ziel unserer Core Facility ist die ständige Erweiterung unseres Analyse-Portfolios auf neue Substanzen oder Substanzklassen im Rahmen biomedizinischer Fragestellungen. Dabei gibt es aber eine Reihe von Aspekten die bei der Erstellung einer neuen Methode zu berücksichtigen sind. So muss z.B. schon zu Beginn der Planungsphase -neben einer prinzipiellen Machbarkeit- überlegt werden, ob der i.d.R. nicht unerhebliche zeitliche, methodische, apparative und nicht zuletzt finanzielle Aufwand, für die Anzahl an geplanten Proben oder die Relevanz des/der Analyten für zukünftige Projekte, gerechtfertigt ist.
Schema einer einfachen Probenvorbereitung mit flüssig-flüssig Extraktion für die GC-MS:

Nach einer mehr oder weniger aufwändigen Probenvorbereitung folgt eine chromatographische Aufreinigung via Flüssigchromatographie (HPLC) oder Gaschromatographie (GC). Die Wahl ist abhängig von jedem einzelnen Analyten, der Probenmatrix in der er vorliegt und seinen individuellen chemisch-physikalischen Eigenschaften (Löslichkeit, Stabilität, Verdampfbarkeit, etc.)
HPLC- und GC-Kapillarsäulen
Links: HPLC-Säulen gefüllt mit 2-5 µm modifiziertem Kieselgel-Trennmaterial
Rechts: GC-Kapillarsäule in einer Länge von 15-100 m mit unterschiedlichen Beschichtungen
Neben der Wahl der Chromatographie ist natürlich auch die Detektionsmethode von entscheidender Bedeutung für eine erfolgreiche Durchführung der Analysen. Jedes unserer einsetzbaren Massenspektrometer weist in den Detektionsmöglichkeiten Unterschiede auf.
Folgende Varianten stehen aktuell zur Verfügung:
GC-MS (SCAN oder SIM [Single Ion] Mode)
EI (Electron Impact; positiv)
GC-MS/MS (SCAN, SIM, Precursor Ion, Product Ion und MRM [Multiple Reaction Monitoring])
EI (positiv), +CI (Chemical Ionisation; positiv), -CI (negativ).
LC-MS/MS - QTRAP
ESI (Electrospray Ionisation) oder APCI (Atmospheric Pressure CI) mit den Methoden:
EMS (Enhanced MS), EMC (Enhanced Multi Charge), EPI (Enhanced Product Ion), ER (Enhanced Resolution), MRM, NL (Neutral Loss), PREC (Precursor Ion), MS2 (Product Ion).
LC-MS/MS - QTOF (Hochauflösende Massenspektrometrie)
ESI oder APCI mit den Methoden:
Q1 Scan, TOF MS, Product Ion, Precursor Ion, IDA Experiment, SWATH Experiment, Pseudo MRM.
Weitere Analyten
Für die Etablierung weiterer Substanzklassen zeigen nachfolgende Verbindungen gute Aussichten analytische Methoden relativ leicht aufbauen zu können:
Zentraler Kohlenstoffmetabolismus (semiquantitativ)
Glucose, Glucose-6-phosphat, Fructose-6-phosphat, Glyceraldehyd-3-phosphat, Fructose-1,6-bisphosphat, DHA(P), 1,3-Bisphosphoglycerat, 3-Phosphoglycerat, Phosphoenolpyruvat.
Kohlenhydrate (semiquantitativ)
Erythrose, Threose, Erythrulose, Arabinose, Ribulose, Ribose, Deoxyribose, Galactose, Mannose, Glucoronsäure, Sucrose, Lactulose, Lactose, Maltose, Glucose-1-phosphat.
Coenzym A (CoA) Derivate (semiquantitativ)
Acetyl-CoA, Malonyl-CoA, ß-Hydroxy-ß-methylglutaryl-CoA (HMG-CoA).
Sonstige Analyten (semiquantitativ)
Arginin, Ornithin, Citrullin, Harnstoff, Ethanolamin, 5-Phosphoribosylamin, Harnsäure, Orotsäure, Xanthin, Hypoxanthin, Adenylosuccinat, Cholesterol, Carbomylphosphat.
Besondere Herausforderungen
Auch spezielle Herausforderungen nehmen wir gerne an.
Einige Darmbakterien sind in der Lage verschiedene Alkohole als Stoffwechselprodukt zu bilden. Diese können dann vom Körper resorbiert werden und u.U. zu erheblichen Problemen bei betroffenen Personen führen. Niedere Alkohole gehören allerdings zu den flüchtigeren Substanzen deren Bestimmung i.d.R. einen besonderen apparativen Aufwand (z.B. Headspace GC-MS) bedarf, der in unserer CF nicht gegeben ist. So sollte mit einem neuen methodischen Ansatz versucht werden Alkohole mittels alternativer LC-MS/MS Methode zunächst qualitativ nachzuweisen.
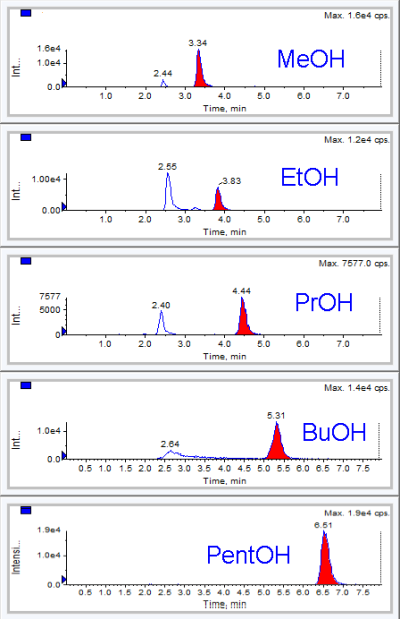
Dieses neue Verfahren ermöglicht nun Alkohole wie Methanol, Ethanol, Propanole, Butan(di)ole oder Pentanole nebeneinander via LC-MS nachzuweisen.
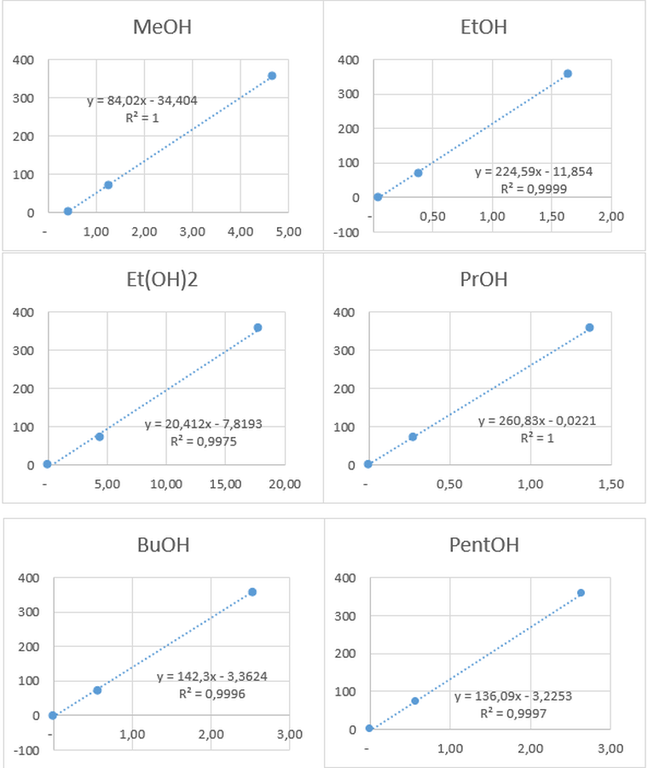
LC-MS/MS-Chromatogramme einer mit verschiedenen Alkoholen gespikten Plasmaprobe
sowie entsprechende 3-Punkt-Kalibrationen zur einfachen Methodenkontrolle
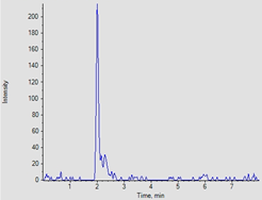
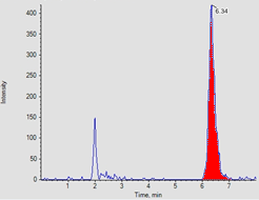
Beispiel: Plasmaprobe zum qualitativen Nachweis von Butandiolen:
Da dies eine Methode mit neuem analytischem Ansatz ist und im Zusammenhang mit möglichen Alkoholsynthesen durch die Darmflora weiterhin von Interesse sein dürfte, soll dieses Verfahren weiterverfolgt und durch Validierung auf analytisch sichere Beine gestellt werden. Darüber hinaus wäre es auch sicher möglich weitere Alkohole in die Methode zu integrieren.
Leider besteht auf Grund der verfahrensbedingten geringen Trennleistung von LC-Säulen das Unvermögen, stukturisomere Alkohole (wie Propanol, Isopropanol, die jeweils vier isomeren Butanole oder Butandiole) chromatographisch voneinander abzutrennen.
Hier könnten die Analyten durch eine weitere Derivatisierung eventuell verdampfbar gemacht werden, um mit der wesentlich höheren Trennleistung der GC-MS-Analytik auch eine Unterscheidung der Strukturisomeren zu erreichen.